臨床研究開発センター
- 2024-6-24
- 診療科・部門紹介
- #治験, #臨床研究開発センター
現在の医療に使われている治療法や治療薬は、その初期の開発段階から有効性や安全性が確認されていたわけではありません。長ければ何十年にも及ぶ研究者の地道な努力と、何よりも研究に対する多くの患者さんの協力があって、現在の実用化が実現しています。
今回は、医療の進歩を支える研究の遂行において重要な役割を担っている三重大学病院の臨床研究開発センターのご紹介です。
それ行け!三重大学病院。それ行け!臨床研究開発センター。科学性、倫理性、信頼性、安全性に基づいた意義ある研究を推進するために。
医療の進歩に欠かせない臨床研究
“今”の医療はこれまでの臨床研究の積み重ね
医療に関わる研究には様々な種類がありますが、中でも人を対象とした研究のことを「臨床研究」といいます。
現在の医療は、こうした過去の臨床研究の積み重ねの結果です。医学の進歩、すなわち新しい医療の開発のために、臨床研究は必要不可欠なものです。

教授 田丸 智巳
様々な臨床研究
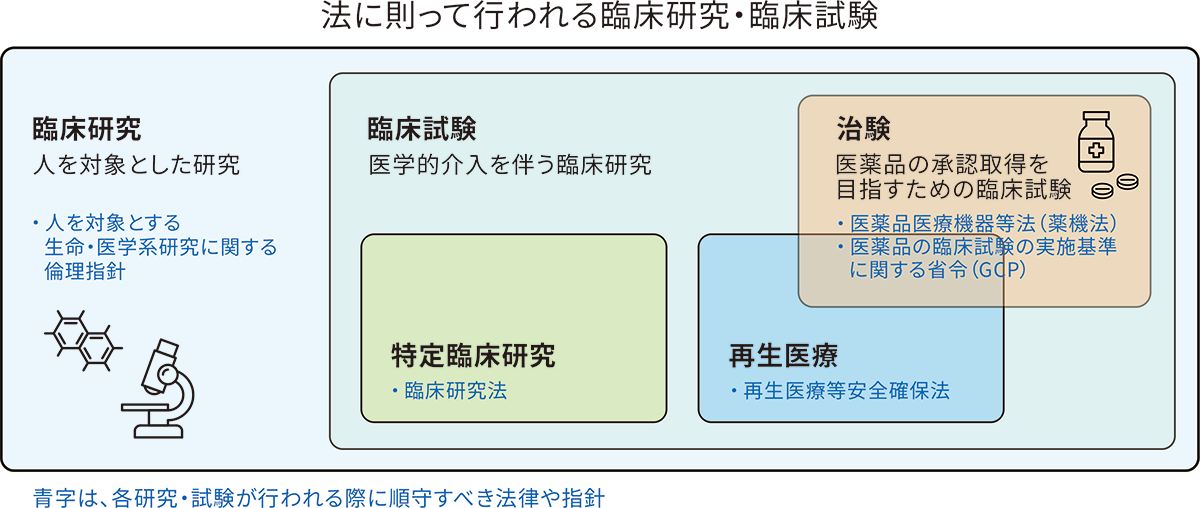
臨床研究は、一般的な診療の範囲内で状態を観察する「観察研究」と、研究のために何らかの医学的判断や処置を伴う「介入研究」に分けられます。臨床研究のうち、この介入研究を「臨床試験」と呼びます。
さらに、臨床試験のうち、「医薬品等の製造販売承認を目的としたもの」が「治験」です。治験は、新しい医薬品が安全で効果のあるものとして、厚生労働省から承認を受けるために行われるものです。
患者さんにとっての臨床試験や治験
治験や臨床試験が治療の選択肢になるとき
基本的に薬物治療を受けられる際には、まず保険診療内で行われるものかどうか、ご確認ください。すでに効果や安全性について厚生労働省が承認をしているお薬であれば、保険診療で行えるようになっているからです。
しかし、すべての疾病や症例で承認薬があるわけではありません。保険診療で使えるお薬では効果が見られず、その中で選択肢がなくなる場合もあります。そんな時、次に検討していただけるのが治験や臨床試験です。
参加にはインフォームド・コンセントが絶対条件
治験は、先にご説明した通り、承認取得を目指すための臨床試験で、それまでにも長い期間をかけて様々な試験が行われ、一定の基準をクリアしてきた薬剤が対象となります。
治験において有効性・安全性が確認できれば、近い将来、厚生労働省に認められたお薬になる予定のものです。
臨床試験には様々な種類がありますが、参加する際には、患者さん自身やご家族が医療機関で詳しい説明を聞き、十分に理解することがとても重要です。このプロセスをインフォームド・コンセントといいます。
同意書にサインする前には、十分なインフォームド・コンセントが不可欠です。疑問がある場合は、必ず担当医に質問してください。
臨床研究に参加していただく意義
冒頭でもお伝えしたように、過去の臨床研究の積み重ねがあって現在の医療があります。臨床研究は、診療とは異なりますが、医学の発展のためにはとても重要なものです。
実施においては、安全を第一として行われますので、臨床研究に対する、みなさまのご理解やご参加をお願いいたします。
三重大学医学部附属病院 臨床研究開発センター
治験遂行の支援
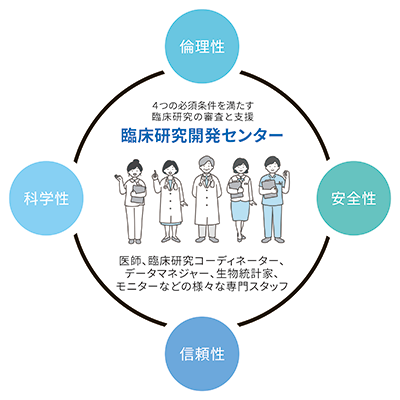
当センターは、設立当初から、治験が科学性、倫理性、安全性、信頼性を満たして行われるように支援を行っています。
特に、治験に参加いただく患者さんが十分にその内容を理解し、不利な立場になることなく意思決定を行えるように、当センターの臨床研究コーディネーター(CRCと呼びます)が、患者さんと医師の間に入って支援をしています。
センターを構成する様々な専門家
臨床研究のうち、特に臨床試験では分業が進んでいます。遂行するのは主に医師ですが、臨床研究専門職と呼ばれるスタッフが様々な過程で大勢関わっています。
臨床研究専門職は、医師と患者さんの間に立って調整・支援を行う「CRC」、臨床試験のデータを管理する「データマネージャー」、データから統計解析を行う「生物統計家」、臨床試験の質を担保するための「モニター」など多岐にわたります。
多職種が関わることで臨床試験を速やかにかつ安全に進めることができています。

医師や研究者が行う臨床研究への協力
また、当院の臨床研究開発センターは、治験のほか、医師や研究者が行う臨床研究についても、計画段階から終了まで適切に遂行されるようサポートしています。
臨床研究を行うにあたっては、国が定めた法律や倫理指針などに従う必要があり、研究を行う者は、必ず倫理委員会の承認を得る必要があります。当センターは、この倫理委員会の事務局となっています。
倫理委員会には、医学・生物学の専門家、一般の方などが委員として参加しており、それぞれの臨床研究の計画について、倫理的に問題がないか、安全性に問題がないかなどを議論し、承認を決定しています。
現在、当院で行われているすべての臨床研究は、この倫理委員会による厳しい審査と承認を経たものです。
なお、当院で行われている臨床研究は、ホームページ(https://www.sv.hosp.mie-u.ac.jp/chiken/public/index/)に掲載し、公表しています。